
Semua kandungan iLive disemak secara perubatan atau fakta diperiksa untuk memastikan ketepatan faktual sebanyak mungkin.
Kami mempunyai garis panduan sumber yang ketat dan hanya memautkan ke tapak media yang bereputasi, institusi penyelidikan akademik dan, apabila mungkin, dikaji semula kajian secara medis. Perhatikan bahawa nombor dalam kurungan ([1], [2], dan lain-lain) boleh diklik pautan ke kajian ini.
Jika anda merasakan bahawa mana-mana kandungan kami tidak tepat, ketinggalan zaman, atau tidak dipersoalkan, sila pilih dan tekan Ctrl + Enter.
Protein utama dikenal pasti untuk mencegah kehilangan jisim tulang dalam osteoporosis
Ulasan terakhir: 02.07.2025
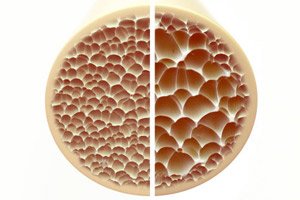
Osteoporosis, keadaan yang dicirikan oleh tulang berliang dan rapuh, menimbulkan ancaman besar kepada kesihatan rangka. Tulang, sebagai sokongan struktur utama tubuh manusia, memberikan sokongan penting. Apabila jisim tulang berkurangan, ia bukan sahaja menjejaskan sokongan ini, tetapi juga menjejaskan fungsi keseluruhan, yang membawa kepada penurunan kualiti hidup.
Apabila insiden osteoporosis meningkat dalam populasi yang semakin tua, terdapat beban yang semakin meningkat pada sumber penjagaan kesihatan untuk penjagaan jangka panjang. Oleh itu, adalah perlu untuk memahami mekanisme yang menyumbang kepada perkembangan osteoporosis dan untuk membangunkan rawatan sasaran yang berkesan untuk meminimumkan kesan jangka panjangnya.
Osteoblas dan osteoklas ialah dua jenis sel yang memainkan peranan penting dalam penyelenggaraan dan pembentukan semula tisu tulang. Walaupun osteoblas ialah sel pembentuk tulang yang bertanggungjawab untuk sintesis dan pemendapan tisu tulang baru, osteoklas ialah sel yang merendahkan tulang yang terlibat dalam pemecahan dan penyingkiran tisu tulang lama atau rosak.
Peningkatan dalam bahagian osteoklas menyebabkan kehilangan tulang dalam keadaan seperti osteoporosis, rheumatoid arthritis (keradangan sendi), dan metastasis tulang (kanser yang telah merebak ke tulang). Osteoklas timbul daripada pembezaan makrofaj atau monosit, yang merupakan jenis sel imun.
Oleh itu, perencatan pembezaan osteoklas boleh berfungsi sebagai strategi terapeutik untuk mencegah kehilangan tulang. Walau bagaimanapun, mekanisme molekul yang tepat yang mengawal proses kompleks pembentukan semula tulang masih tidak jelas.
Dalam kajian baharu, Profesor Tadayoshi Hayata, Encik Takuto Konno dan Cik Hitomi Murachi dari Universiti Sains Tokyo, bersama-sama rakan sekerja, menyelidiki peraturan molekul pembezaan osteoklas. Rangsangan dengan pengaktif reseptor ligan kappa B faktor nuklear (RANKL) mendorong pembezaan makrofaj kepada osteoklas.
Di samping itu, laluan isyarat protein morfogenetik tulang (BMP) dan faktor pertumbuhan berubah (TGF) -β telah terlibat dalam pengawalseliaan pembezaan osteoklas yang dimediasi RANKL. Dalam kajian semasa, penyelidik bertujuan untuk menyiasat peranan Ctdnep1, fosfatase (enzim yang menghilangkan kumpulan fosfat) yang telah dilaporkan untuk menindas laluan isyarat BMP dan TGF-β.
Kajian itu diterbitkan dalam jurnal Biochemical and Biophysical Research Communications.
Profesor Hayata menyatakan: "RANKL bertindak sebagai 'pemecut' untuk pembezaan osteoklas. Memandu kereta memerlukan bukan sahaja pemecut tetapi juga brek. Di sini, kami mendapati bahawa Ctdnep1 bertindak sebagai 'brek' dalam pembezaan osteoklas."
Para penyelidik mula-mula memeriksa ekspresi Ctdnep1 dalam makrofaj tikus yang dirawat RANKL dan sel kawalan yang tidak dirawat. Mereka memerhatikan bahawa ekspresi Ctdnep1 tidak berubah sebagai tindak balas kepada rangsangan RANKL. Walau bagaimanapun, ia disetempatkan kepada sitoplasma dalam bentuk berbutir dalam makrofaj dan dibezakan kepada osteoklas, berbeza daripada penyetempatan perinuklear biasa dalam jenis sel lain, menunjukkan fungsi sitoplasmanya dalam pembezaan osteoklas.
Tambahan pula, penurunan Ctdnep1 (menurunkan regulasi ekspresi gen) mengakibatkan peningkatan dalam bilangan osteoklas yang positif untuk fosfatase asid tahan tartrat (TRAP), di mana TRAP ialah penanda osteoklas yang berbeza.
Kalah mati Ctdnep1 mengakibatkan peningkatan ekspresi penanda pembezaan utama, termasuk "Nfatc1," faktor transkripsi induk yang disebabkan oleh RANKL untuk pembezaan osteoklas. Keputusan ini menyokong "fungsi brek" Ctdnep1, di mana ia mengawal selia pembezaan osteoklas secara negatif. Selain itu, kalah mati Ctdnep1 juga mengakibatkan peningkatan penyerapan kalsium fosfat, mencadangkan peranan menindas untuk Ctdnep1 dalam penyerapan tulang.
Akhirnya, walaupun kalah mati Ctdnep1 tidak mengubah isyarat BMP dan TGF-β, sel kekurangan Ctdnep1 menunjukkan peningkatan tahap protein terfosforilasi (diaktifkan), yang merupakan produk laluan isyarat RANKL. Keputusan ini menunjukkan bahawa kesan perencatan Ctdnep1 pada pembezaan osteoklas mungkin tidak dimediasi melalui isyarat BMP dan TGF-β, tetapi melalui downregulation laluan isyarat RANKL dan tahap protein Nfatc1.
Secara keseluruhan, keputusan ini memberikan pandangan baharu tentang proses pembezaan osteoklas dan mengenal pasti sasaran terapeutik yang berpotensi yang boleh digunakan untuk membangunkan rawatan untuk mengurangkan kehilangan tulang akibat terlalu aktif osteoklas. Sebagai tambahan kepada penyakit yang dicirikan oleh kehilangan tulang, Ctdnep1 juga telah dikenal pasti sebagai faktor penyebab medulloblastoma, tumor otak kanak-kanak. Penulis optimis bahawa penyelidikan mereka boleh diperluaskan kepada penyakit manusia lain di luar metabolisme tulang.
Profesor Hayata menyimpulkan: "Keputusan kami mencadangkan bahawa Ctdnep1 diperlukan untuk mencegah osteoklastogenesis yang berlebihan. Keputusan ini boleh mengembangkan lagi pengetahuan kami tentang bagaimana rangkaian fosforilasi-defosforilasi mengawal pembezaan osteoklas dan mungkin menyediakan strategi terapeutik baru untuk rawatan penyakit tulang yang berkaitan dengan aktiviti osteoklas yang berlebihan."
